代谢异常是癌症的重要特征之一,挖掘癌症代谢异常的调控机制对阐明癌症发生发展的分子机制具有重大意义。其中,精氨酸可通过影响代谢重编程以促进肿瘤的生长。然而,关于肿瘤细胞精氨酸代谢的调控机制尚未完全阐明。
近日,一项发表于 Cell 的研究通过肝细胞癌(HCC)小鼠模型进行非靶向代谢组学、转录组学、蛋白质组学等多方面的研究,揭示了 精氨酸驱动肿瘤代谢的关键机制。为肝癌治疗提供了新的途径,快和小陶一起来看看吧~

▲原文截图
为了揭示 HCC 中的代谢变化,研究人员首先利用 mTOR 驱动的 HCC 小鼠模型中分离的肝肿瘤进行了非靶向代谢组学研究。观察到 L-dKO(特异性肿瘤抑制基因TSC1和PTEN双基因敲除)肿瘤中发生了明显的精氨酸代谢改变——肿瘤细胞中精氨酸水平显著升高(肿瘤细胞本身很少或不产生精氨酸),且高水平的精氨酸是肿瘤生长所必需的。
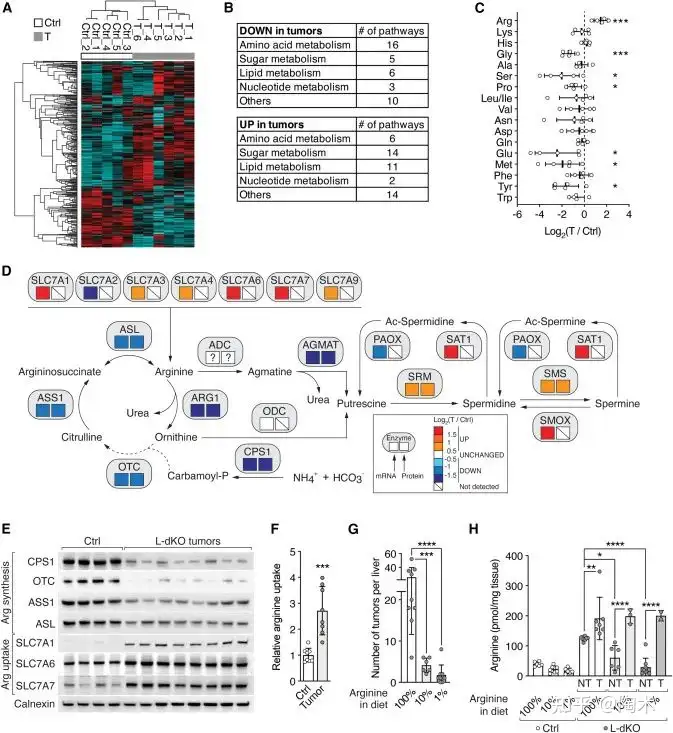
▲精氨酸在肝脏肿瘤中升高,促进肿瘤形成
精氨酸如何导致致瘤性?精氨酸是一种多功能的氨基酸,不仅是蛋白质合成的基本组成部分,还是多胺、肌酸和一氧化氮的前体。在小鼠实验中,由于肝癌小鼠受到尿素循环通路的抑制,导致精氨酸合成减少,但肿瘤能够通过增加精氨酸的摄取来弥补这一不足。因此,当研究人员将小鼠 饮食中的精氨酸水平降低至正常水平的 10% 或 1% 时,肝癌小鼠的肿瘤负荷明显减少,这表明精氨酸对于肿瘤的发展至关重要。
此外,肿瘤细胞之所以能够维持高浓度的精氨酸,是通过增加摄取并减少向多胺的转化来实现的。在 L-dKO 小鼠中,研究人员观察到肿瘤细胞中多胺代谢酶的表达发生了变化,具体表现为精氨酸酶1(ARG1)和胍丁胺酶(AGMAT)的转录水平下调,抑制了它们催化精氨酸向多胺的转化途径,从而减少了精氨酸的消耗。与此同时,这一变化诱导了天冬氨酸合成酶(ASNS)的表达和天冬酰胺的产生,促进了精氨酸的摄取,从而保持了高水平未代谢的精氨酸存在。
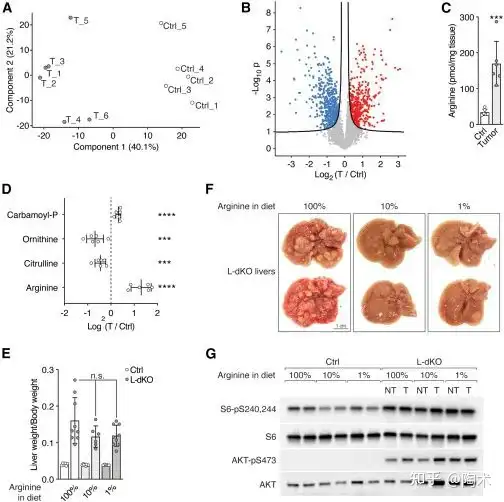
▲ARG1和AGMAT的缺失促进了肝脏肿瘤的形成
进一步,研究人员选择 SNU449 细胞系建立了一个模拟 L-dKO 肿瘤的体外试验系统,以探究精氨酸水平的致瘤性。实验发现,在肝癌细胞中,RBM39 作为转录共调节因子,特异性地与精氨酸结合,从而调节代谢基因的表达。
PS: RBM39 是一种 RNA 结合蛋白,参与转录共调控和选择性 RNA 剪接。其降解会导致异常剪接和差异基因表达,从而抑制细胞周期进程并导致肿瘤消退。
RBM39 的缺失或精氨酸限制(即ARG1/AGMAT表达下调)可以降低代谢基因的表达,包括 ASNS、PSAT1、PSPH、GLSK、GLUT3、HK2、NNMT 和 AOC3 等。这表明RBM39 可以通过转录控制代谢基因的表达,从而影响肝癌细胞的代谢重编程。此外,RBM39 的表达水平升高可以促进 ASNS 的表达,从而增加精氨酸的摄取,进一步重编程代谢通路,从而促进肝癌的发生。
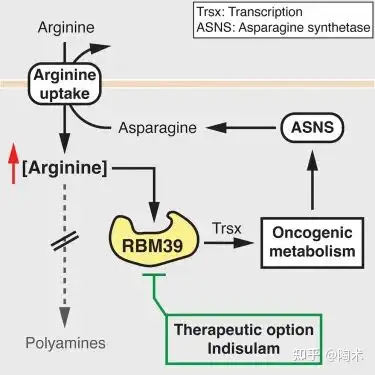
▲高浓度精氨酸通过结合RBM39重编程癌细胞代谢
肝癌新疗法?既然精氨酸可以结合 RBM39 改变代谢相关基因的转录来促进肿瘤的发展,那是否可以靶向此途径来消除肿瘤呢?
带着这个疑问,研究人员分析了来自肝癌患者的肿瘤和相邻非肿瘤组织生物样本的蛋白质组和转录组。发现与小鼠肝癌模型中观察到的类似,肝癌患者的肿瘤表现出尿素循环受抑制、多个精氨酸转运蛋白上调以及多胺生物合成酶失调等特征。尤其是在侵袭性肝癌中,ARG1 和 AGMAT 的表达降低,而 RBM39 和 ASNS 的表达增加。
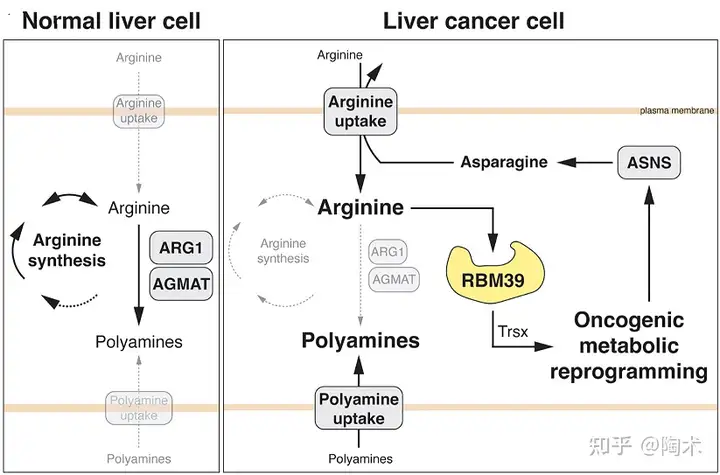
▲ARG1, AGMAT,精氨酸和RBM39在人类HCC患者中的作用
接下来,研究人员利用可降解 RBM39 的药物indisulam处理了源自 20 个患者的 HCC 类器官样本,发现Indisulam以剂量依赖的方式遏制了所有类器官的生长。表明RBM39 的耗竭可能是治疗 HCC 的一个选择。
小结总的来说,肿瘤细胞通过增加精氨酸的摄入并减少其向多胺的转化,从而积累高水平的精氨酸。这种高水平的精氨酸重新编程了代谢,进而促进了肿瘤的发展。精氨酸通过结合到 RBM39,控制代谢基因的表达,尤其是通过促进 ASNS 的表达,从而刺激天冬氨酸的合成,进一步加强了对精氨酸的吸收,形成了一个正反馈循环,维持了高精氨酸水平和致癌代谢。
此外,研究还提出了以 RBM39 为靶点的潜在癌症治疗策略。RBM39 的缺失或精氨酸限制可以降低代谢基因的表达,包括 ASNS、PSAT1、PSPH、GLSK、GLUT3、HK2、NNMT 和 AOC3 等,并抑制肝癌的进展。综上,这项研究深入探讨了肝癌代谢重编程的机制,并确定了 RBM39 作为潜在的治疗靶点,为肝癌治疗提供了新的希望。
当下,癌症代谢相关研究如火如荼,陶术生物拥有 800+化合物库,其中有一些是致力于癌症代谢异常相关研究的,例如 抗肝癌化合物库 、代谢化合物库、转录因子化合物库、细胞重编程化合物库 等,欢迎私信咨询~




参考资料:
[1] Mossmann D, Müller C, Park S, et al. Arginine reprograms metabolism in liver cancer via RBM39 [published online ahead of print, 2023 Sep 26]. Cell. 2023;S0092-8674(23)01032-2. doi:10.1016/j.cell.2023.09.011
[2] Scientists discover arginine drives metabolic reprogramming to promote tumor growth in liver cancer. https://medicalxpress.com/news/2023-10-scientists-arginine-metabolic-reprogramming-tumor.html
 |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033