金币
UID846032
帖子
主题
积分156
注册时间2022-10-12
最后登录1970-1-1
听众
性别保密
|
欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
在2023年版GMP指南-厂房设施与设备的4.2.2.4 美国 cGMP对制药用水系统的要求中提到:
“美国FDA 《高纯水系统检查指南》对制药用水的一些关键性要求如下:要求死角最少;不推荐注射用水回路的用点处安装过滤器;推荐注射用水分配 系统管道材质为316L不锈钢;推荐换热器采用双端板设计或采用压差监测;要求储罐采用呼吸器,防止外界污染;管道坡度需符合要求;使用卫生型离心泵;批处理状态下,静止保存的注射用水必须在24小时内使用;”
在美国FDA 《高纯水系统检查指南》中与之相关的内容是:
X. REVERSE OSMOSIS
X.反渗透
With the development of biotechnology products, many small companies are utilizing RO and UF systems to produce high purity water. For example, Figure 9 illustrates a wall mounted system that is fed by a single pass RO unit.
随着生物技术产品的发展,许多小公司正在利用反渗透和超滤系统生产高纯水。例如,图9显示了一个由单通道反渗透装置供电的壁挂式系统。
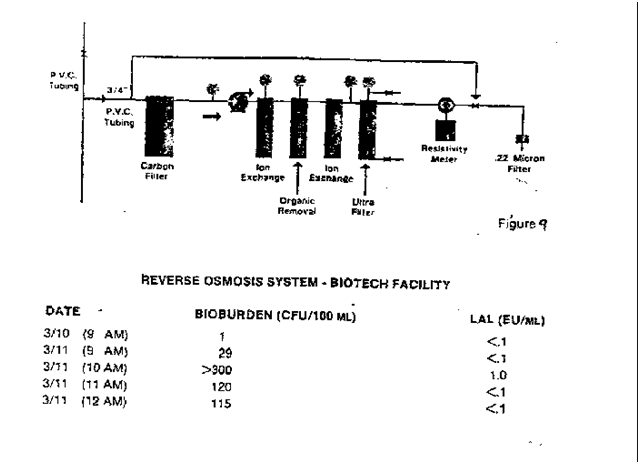
As illustrated, most of these systems employ PVC or some type of plastic tubing. Because the systems are typically cold, the many joints in the system are subject to contamination. Another potential problem with PVC tubing is extractables. Looking at the WFI from a system to assure that it meets USP requirements without some assurance that there are no extractables would not be acceptable.
如图所示,这些系统大多采用PVC或某种类型的塑料管。由于这些系统通常很冷,系统中的许多接头都容易受到污染。PVC管的另一个潜在问题是可提取物。从系统中查看WFI以确保其符合USP要求,而不保证没有可提取物,这是不可接受的。
The systems also contain 0.2 micron point of use filters which can mask the level of microbiological contamination in the system. While it is recognized that endotoxins are the primary concern in such a system, a filter will reduce microbiological contamination, but not necessarily endotoxin contamination. If filters are used in a water system there should be a stated purpose for the filter, i.e., particulate removal or microbial reduction, and an SOP stating the frequency with which the filter is to be changed which is based on data generated during the validation of the system.
该系统还包含0.2微米的使用点过滤器,可以掩盖系统中的微生物污染水平。虽然人们认识到内毒素是这种系统中的主要问题,但过滤器可以减少微生物污染,但不一定是内毒素污染。如果在水系统中使用过滤器,则应明确过滤器的用途,即去除颗粒物或减少微生物,并制定SOP,说明根据系统验证期间生成的数据更换过滤器的频率。
As previously discussed, because of the volume of water actually tested (.1ml for endotoxins vs. 100ml for WFI), the microbiological test offers a good index of the level of contamination in a system. Therefore, unless the water is sampled prior to the final 0.2 micron filter, microbiological testing will have little meaning.
如前所述,由于实际测试的水量(内毒素为0.1ml,注射用水为100ml),微生物测试为系统中的污染水平提供了一个很好的指标。因此,除非在最终的0.2微米过滤器之前对水进行取样,否则微生物检测将毫无意义。
At a reinspection of this facility, it was noted that they corrected the deficient water system with a circulating stainless steel piping system that was fed by four RO units in series. Because this manufacturer did not have a need for a large amount of water (the total system capacity was about 30 gallons), they attempted to let the system sit for approximately one day. Figure 9 shows that at zero time (at 9 AM on 3/10), there were no detectable levels of microorganisms and of endotoxins. After one day, this static non-circulating system was found to be contaminated. The four consecutive one hour samples also illustrate the variability among samples taken from a system. After the last sample at 12 PM was collected, the system was resanitized with 0.5% peroxide solution, flushed, recirculated and resampled. No levels of microbiological contamination were found on daily samples after the system was put back in operation. This is the reason the agency has recommended that non-recirculating water systems be drained daily and water not be allowed to sit in the system.
在对该设施进行重新检查时,注意到他们用由四个串联的反渗透装置供给的循环不锈钢管道系统纠正了缺水系统。由于该制造商不需要大量的水(系统总容量约为30加仑),他们试图让系统静置约一天。图9显示,在零时间(3/10上午9点),没有可检测到的微生物和内毒素水平。一天后,发现这个静态非循环系统被污染了。连续四个一小时的样本也说明了从系统中采集的样本之间的可变性。在收集了下午12点的最后一个样品后,用0.5%的过氧化物溶液对系统进行重新初始化、冲洗、再循环和重新取样。系统重新投入运行后,每日样本中未发现微生物污染水平。这就是该机构建议每天排空非再循环水系统,不允许水进入系统的原因。
所以其实美国FDA 《高纯水系统检查指南》并没有进行明确的要求,想知道哪些法规指南提到静止保存的注射用水必须在24小时内使用
我知道答案
回答被采纳将会获得 10 金币 + 60 金币 已有4人回答
|
|
 |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033