欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
无菌过滤系统完整性测试方法
撰稿人:田耀华改编 备注:原作 朱玉洁 梁毅
摘 要:通过对完整性测试原理的探讨,各种完整性测试操作方法及其适用性的研究,对企业提出一些操作性建议。
关键词:完整性测试;起泡点测试;扩散流测试;HydroCorr测试
无菌产品制造分为两类:第一类是产品最终灭菌型,第二类是非最终灭菌型。无菌制剂的灭菌是整个产品在生产过程中的关键,对于热敏性程度比较高的药品,由于不能进行热力灭菌而大多采用无菌过滤的方法进行微生物的滤除。在无菌过滤过程中,过滤器是工艺中最关键的组件之一,它和终端灭菌工艺中的灭菌釜同样重要,为最终产品提供无菌保障。无菌过滤的效果取决于过滤器的特性和完整性测试的效果[1][2]。完整性测试是保证无菌过滤系统有效的必需手段,也在法规中作了明确要求。
1完整性测试概述
有两个基本的理由需要做完整性测试,需要做一系列测试,例如:确认制造规格、正确的过滤孔径、灭菌前的完整性和蒸汽、消毒灭菌后的完整性等,保证产品达到相应的质量要求,易于被客户接受;另一方面,从法规角度看,过滤是操作的关键步骤,从质量管理的宗旨出发,保证过滤系统的有效性就必须要求进行滤膜的完整性测试。




HydroCorr的专用测试适用于疏水型呼吸过滤器SIP以后过滤前的完整性测试。此种测试是在呼吸过滤器的上部而不要求在其下部进行操作,因而完全适用于对过滤器的完整性评价及SIP的在线灭菌过程,且不致损坏呼吸过滤器。
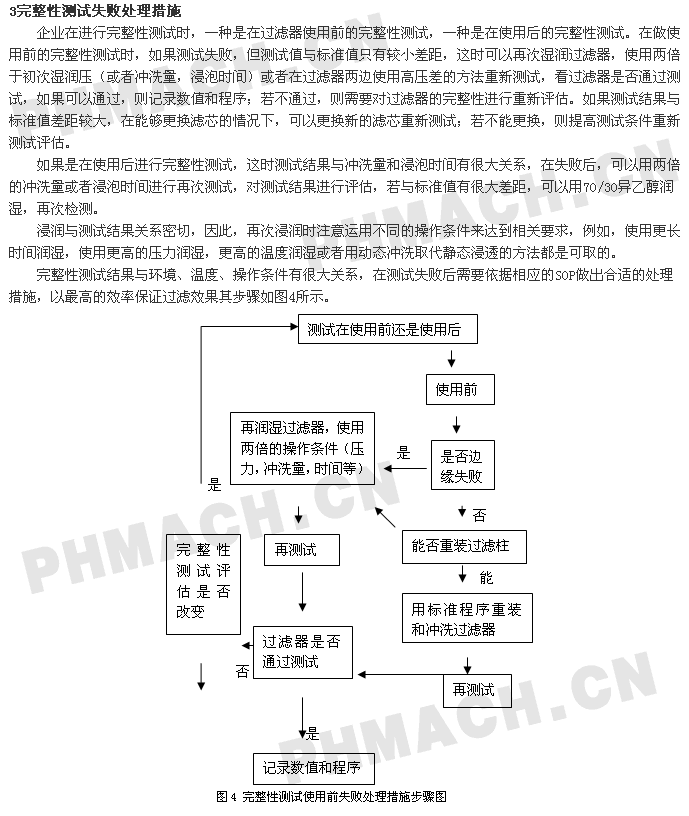 参考文献
参考文献:朱玉洁,梁毅.无菌过滤系统完整性测试方法探讨. 中国制药装备[J].总59期.2010(7)
|  |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033