欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
导读 在《中华人民共和国药品管理法》中,药品上市许可持有人是指取得药品注册证书的企业或者药品研制机构等【1】。而药品上市许可持有人(MAH,Marketing Authorization Holder)制度通常指拥有药品技术的药品研发机构或者药品生产企业主体,通过提出药品上市许可申请获得药品上市许可批件,并对药品质量在其整个生命周期内承担主要责任的制度。
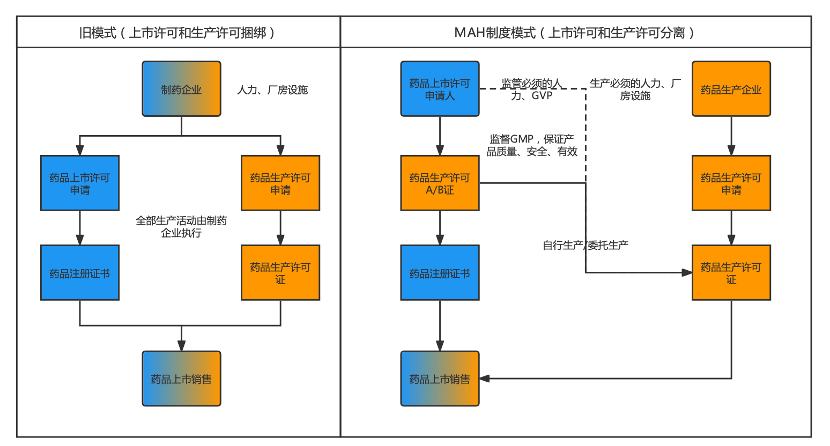
图1 药品生产及上市的新旧模式对比(可点击图片放大化)那么,MAH是如何来的呢? 在历史上,MAH制度最早是由欧美发达国家探索建立。而中国自上世纪80年代以来一直实行药品上市许可与生产许可合并的管理模式,从2015年下半年开始,一系列MAH制度的相关法规政策相继出台,逐步形成以药品上市许可持有人制度为中心的新制度。 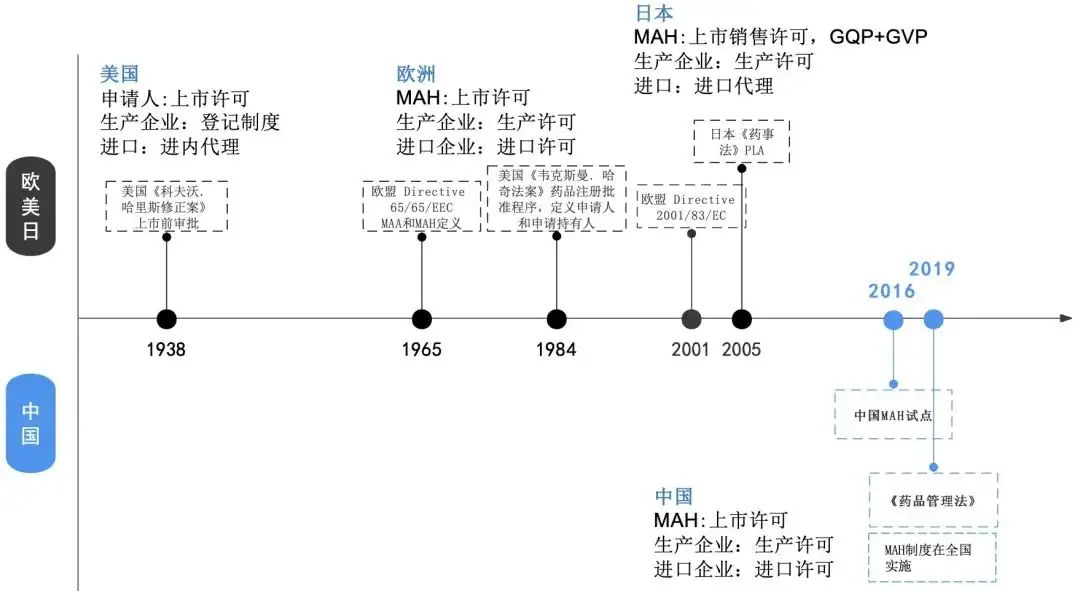
图2 MAH制度发展时间线(可点击图片放大化)在MAH的发展过程中,中国、欧洲、美国、日本各国家都是根据自己的国情情况形成了各具本土特色的MAH制度。那么,下面将详细列举出它们各自的主要区别(可点击下方图片放大化哦): 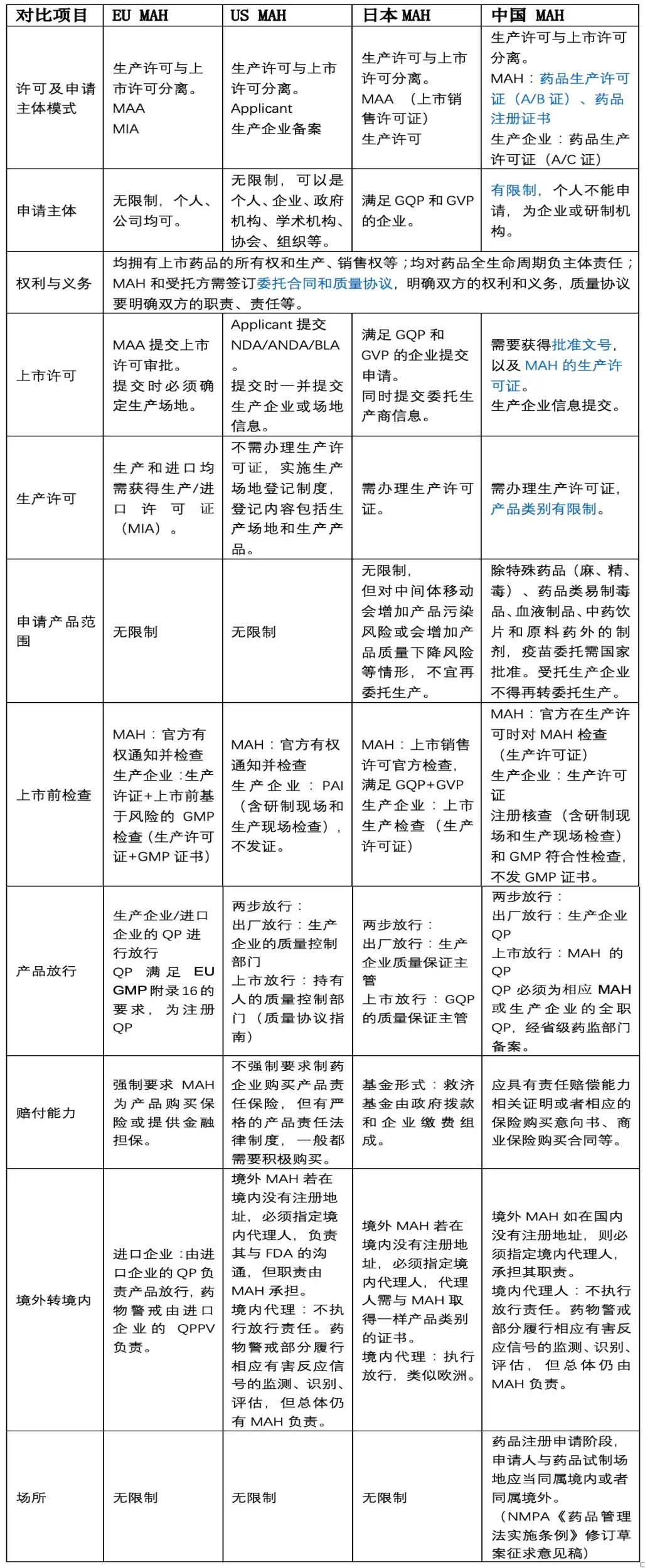 到此,您是否对MAH的发展以及主要国家的MAH制度有了更进一步的了解呢?如您对本文或者MAH主题内容感兴趣,可在下方给我们留言哦。 另外,在接下来的文章中,我们会继续推出MAH一系列文章。如您有兴趣,可关注我们,不错过每一期的精彩~ 参考资料 1. 《中华人民共和国药品管理法》
END
|  |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033