金币
UID938412
帖子
主题
积分21
注册时间2024-2-4
最后登录1970-1-1
听众
性别保密
|
欢迎您注册蒲公英
您需要 登录 才可以下载或查看,没有帐号?立即注册
x
本帖最后由 SUNGO小袁 于 2024-3-2 15:20 编辑
ANVISA对于医疗器械的主要要求:
•所有在巴西进口或分销的医疗器械,必需进行ANVISA认证;
•ANVISA认证后,产品认证结果会公布在Brazil‘s Official Diary (DOU)日报;
•完成ANVISA认证后,产品会列出ANVISA数据库;
•除了ANVISA认证,某些产品需要INMERTO/ANATEL认证;
产品分类:Class 1/Class 2/Class 3/Class 4
分类规则:Resolution - RDC No.751, Attachment 1(和MDR分类规则基本一致;)
巴西医疗器械注册术语:
ANVISA-Brazil National Health Surveillance Agency巴西国家卫生监督局
BGMP-Brazilian Good Manufacturing Practice巴西良好制造规范
INMETRO- 巴西国家计量、质量和技术研究院
ANATEL-巴西通讯管理局
INCQS-巴西国家卫生质量控制研究所
巴西ANVISA认证步骤具体流程 :
1 确认产品分类 *:确认产品分类,以及是否需要进行额外的认证和检测
2 准备资料清单
3 客户根据要求准备资料 : 若判定需要额外认证,需要开始安排
4 GMP申请:仅适用于3和4类器械
5 INMERTO认证:仅适用于有源器械,植入类器械等
6 ANATEL认证:仅适用于有通讯功能的器械
7 编写技术文件: 步骤7可以和步骤4-6同步进行
8 提交注册申请,官方审批
9 审批完成
证书有效期: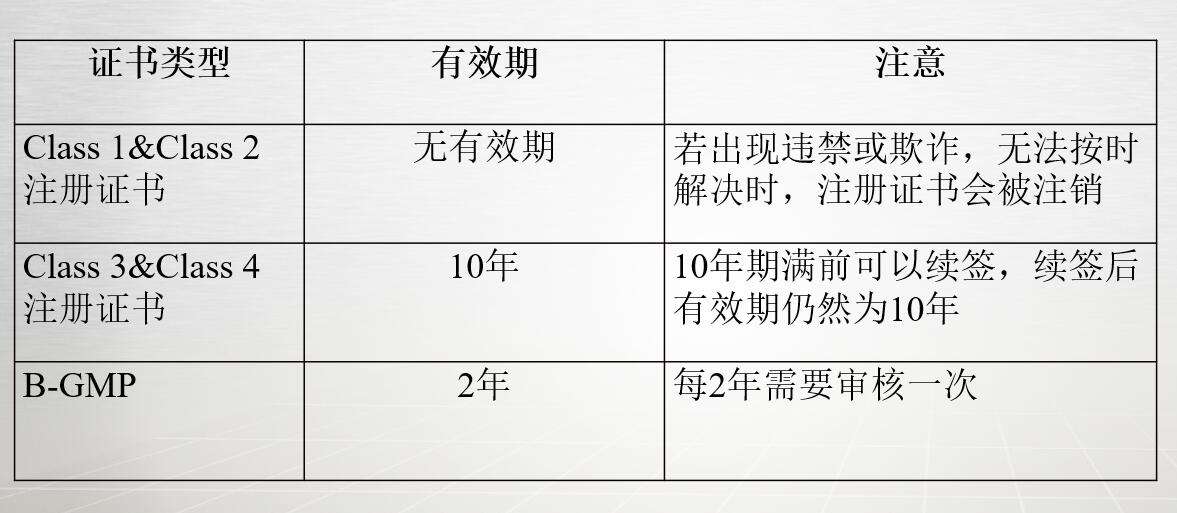
|
|
 |手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033
|手机版|蒲公英|ouryao|蒲公英
( 京ICP备14042168号-1 ) 增值电信业务经营许可证编号:京B2-20243455 互联网药品信息服务资格证书编号:(京)-非经营性-2024-0033