集采背景下,原料药市场将迎来大变局?

2021年是实施"十四五"规划、是国内全面开启建设药品"全生命"周期监管要求新征程的第一年。2021年11月3日,医药界朋友们各大朋友圈、网络平台被《关于启用短缺药品生产供应及停产报告信息采集模块的通知》和《关于启用原料药生产供应告信息采集模块的通知》的消息疯狂刷屏,让我们再次看到了国家药监局进一步做好短缺药品保供稳价工作,深化医药改革的决心。该公告自通知印发之日(2021年11月3日)起正式启用。国家药监局在药品信息采集平台中开发建设了短缺药品生产供应及停产报告信息采集模块,对在我国境内制剂企业和原料药生产企业具有深远的意义。
一、让短缺药品买得到、用得起!
新《药品管理法》自2019年12月1日起实施,明确了国家实行短缺药品清单管理制度,为国家短缺药品供应提供了制度保障,后续国务院办公厅发布《关于进一步做好短缺药品保供稳价工作的意见》(国办发〔2019〕47号),《国家短缺药品清单管理办法(试行)》建立健全短缺药品清单管理制度;为了进一步做好短缺药品清单管理工作,2020年12月30日,国家卫生健康委办公厅等部门发布《关于印发国家短缺药品清单的通知》(以下简称通知),并公布了国家短缺药品清单和临床必需易短缺药品重点监测清单。
2020年以来,新冠疫情、原料药的供应短缺、药品的价格低导致企业的生产意愿低、环保问题等影响原料药产业的众多因素正在以前所未有的力度影响药品供应。据报道,目前我国已成为全球第一大原料药生产大国,随着短缺药品清单管理制度逐步建立健全,我国药品短缺矛盾有所缓解,大范围、长期性短缺情况较少,主要是暂时性、局部性短缺;为了让短缺药品买得到、用得起,2020年12月30日,国家卫生健康委办公厅、国家发展改革委办公厅、国家医疗保障局办公室等12个部门联合印发《印发国家短缺药品清单》和《国家临床必需易短缺药品重点监测清单》,要求各省级联动机制牵头单位要会同相关部门做好国家清单中药品的供应保障工作。
二、落实短缺药品停产报告程序
2019年10月11日,国务院办公厅发布《关于进一步做好短缺药品保供稳价工作的意见》(国办发〔2019〕47号)(成文日期:2019年09月25日),明确要求国家卫生健康委、国家医保局、国家药监局分别负责,工业和信息化部等参与,2019年12月底前实施短缺药品停产报告,省级联动机制牵头单位对省级短缺药品清单中的药品进行评估,认为需进行停产报告的,按规定及时报告国家联动机制牵头单位。国家联动机制牵头单位会同相关部门综合论证省级上报的药品和国家短缺药品清单中的药品,对确需进行停产报告的短缺药品,应向社会发布公告并动态调整。药品上市许可持有人停止生产短缺药品的,应按照规定向国务院或省级人民政府药品监督管理部门报告,药品监督管理部门接到报告后按规定及时通报同级联动机制牵头单位。以上具体规定和时限要求由国家联动机制牵头单位、国家药监局按职责分别制定。医疗保障部门应根据既往平台采购信息,及时向同级联动机制牵头单位报告停产对市场供给形势的影响。卫生健康部门应根据医疗机构既往临床使用信息,及时研判停产药品短缺风险。
三、新政下受影响的原料药有哪些?
国家药监局综合司《关于启用短缺药品生产供应及停产报告信息采集模块的通知》和《关于启用原料药生产供应告信息采集模块的通知》涉及的两个模块信息采集工作聚焦于《国家短缺药品清单》《国家临床必需易短缺药品重点监测清单》的63个品种,其他品种及其原料药暂无要求。以上两个清单来源于2020年12月30日,国家卫生健康委办公厅、国家发展改革委办公厅、国家医疗保障局办公室等12个部门联合印发《印发国家短缺药品清单》和《国家临床必需易短缺药品重点监测清单》,清单如下:
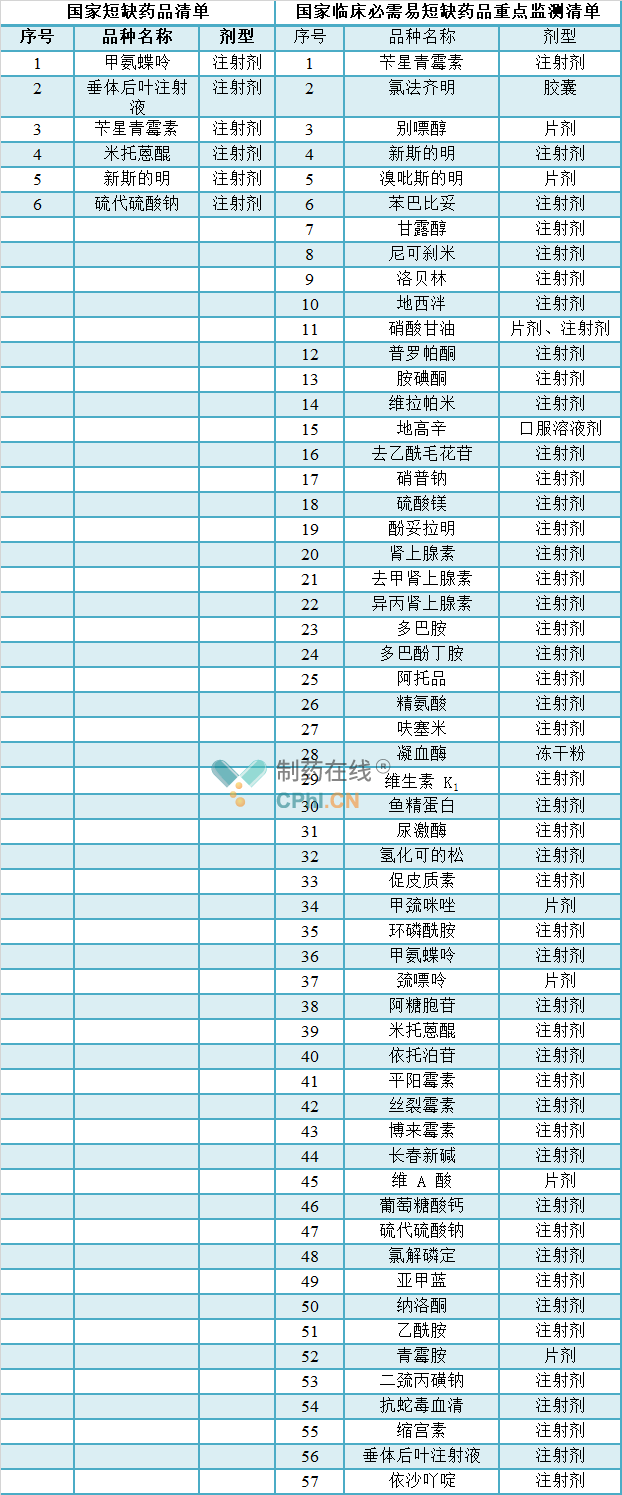
四、新集采时代,原料药国内关联审评审批情况如何查询?
原料药是药品不可分割的重要组成部分,与药品质量安全息息相关。2016年8月10日国家食品药品监督管理总局发布了《总局关于药包材药用辅料与药品关联审评审批有关事项的公告》(2016年第134号),正式官宣我国原辅包的注册从单独审评审批(批准文号管理)正式改革为以备案管理为手段的原辅包与药品关联审评审批的管理模式。
集采之后,原料药行业洗牌将至。集采对供应量的考核要求下,因为原材料短缺,对于集采保供的企业是致命的,所以制剂企业对上游原料采购策略上有了质的变化。以前对于原料药品种和公司随便挑,如今找到一家公司就得先签三年的合作协议。那么医药人如何查询短缺药品的原料药国内关联审评审批情况呢?首先登入国家药品监督管理局药品审评中心(https://www.cde.org.cn/),点击信息公开-选择"原辅包登记信息",界面示例如下图:
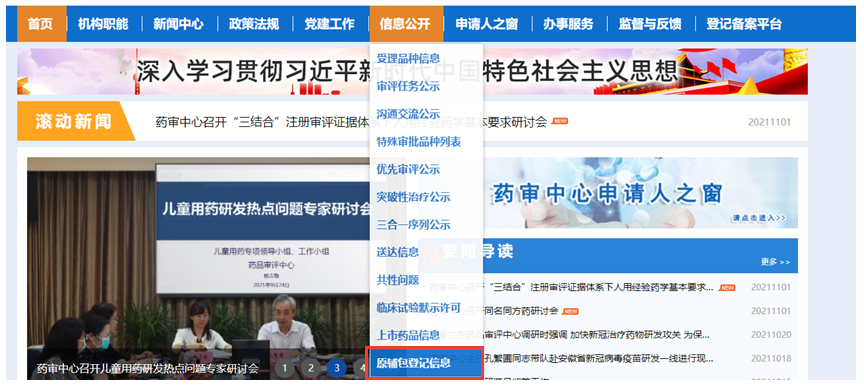
在查询条件右边栏目,输入国家短缺药品-甲氨蝶呤,查出国内有7家企业已经登记,并且与制剂共同审批结果都是A类。
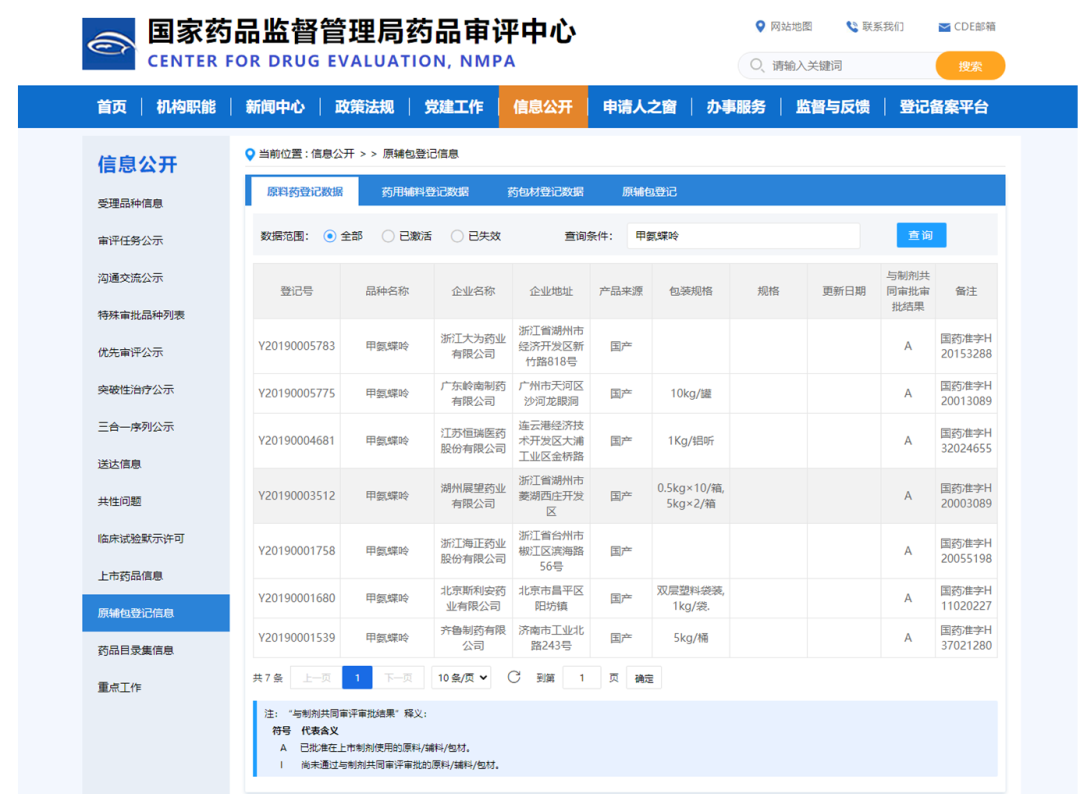
参考文献
[1] www.nmpa.gov.cn
[2] www.cde.org.cn
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/rEvlda11l3j-sh3Xhd6_jQ)



