飞检不合格,7家企业被通报
3月25日,国家药监局食品药品审核查验中心发布了《医疗器械飞行检查情况通告》。
通报内容显示:依据《医疗器械监督管理条例》《医疗器械生产监督管理办法》《药品医疗器械飞行检查办法》《医疗器械生产质量管理规范》及相关附录,以及《食品药品监管总局关于印发医疗器械生产质量管理规范现场检查指导原则等4个指导原则的通知》(食药监械监〔2015〕218号)等要求,按照国家药品监督管理局2021年医疗器械检查工作部署,核查中心于2021年10月-12月组织开展了医疗器械生产企业飞行检查工作,发现有7家企业存在一般项目不符合《医疗器械生产质量管理规范》及相关附录要求。
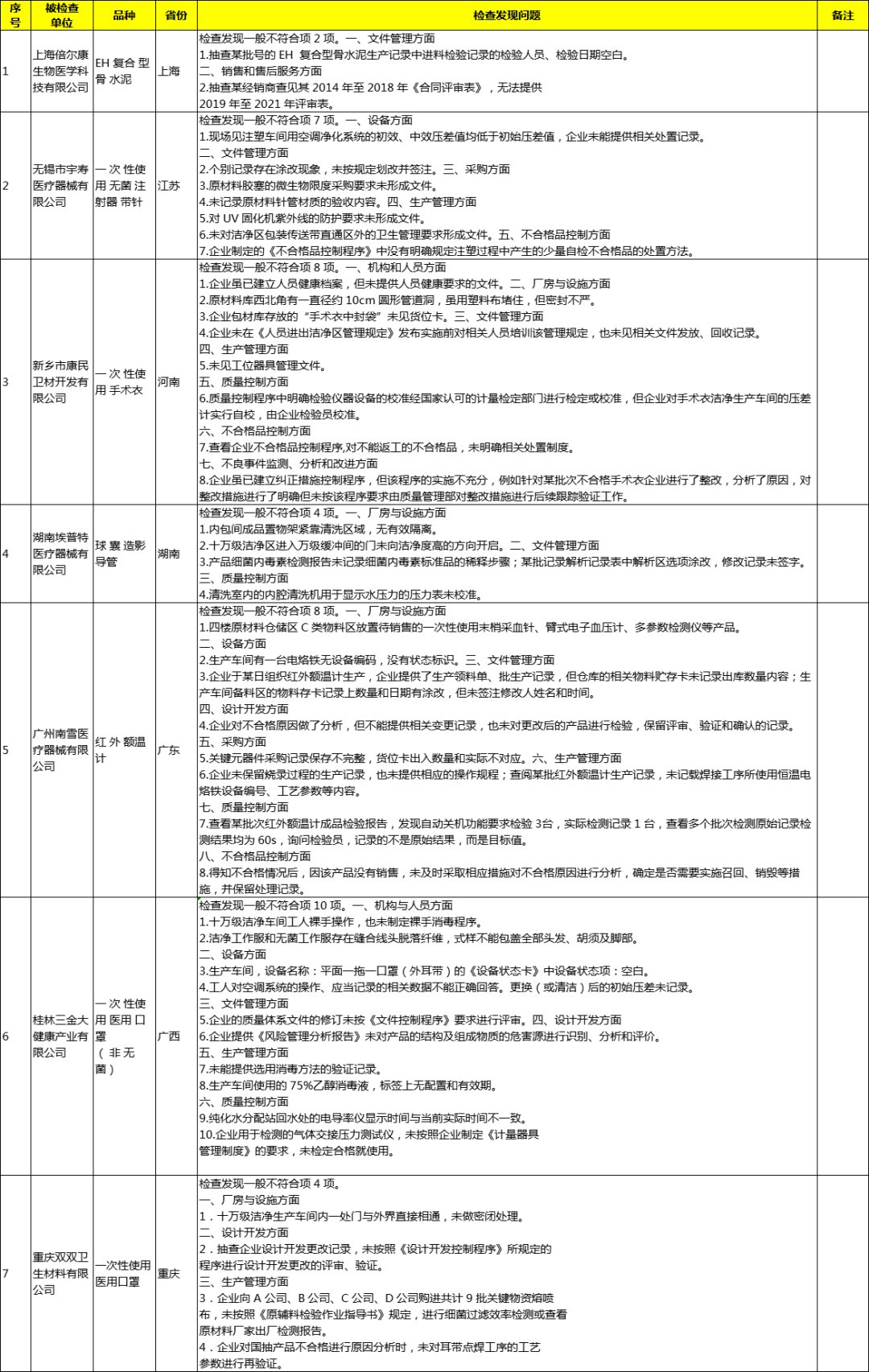
根据审核查验中心公布的飞检情况来看,上海倍尔康生物医学科技有限公司、无锡市宇寿医疗器械有限公司、新乡市康民卫材开发有限公司、湖南埃普特医疗器械有限公司、广州南雪医疗器械有限公司、桂林三金大健康产业有限公司、重庆双双卫生材料有限公司7家医疗器械企业存在不符合项目,检查发现不符合项共计43项。本次飞检品种中,包括一次性使用医用口罩、红外额温计、球囊造影导管、一 次性使用手术衣、一次性使用无菌注射器带针、EH复合型骨水泥。
值得注意的是,广州南雪医疗器械有限公司此次被查处不合格项目多达8项,涉及质量控制、生产管理等方面。其中在今年3月份期间,该公司生产的红外额温计被检测出不合格,因此,被广州市场监督局处以2.5万元的罚款;并且在2020年期间,生产的电子体温计、红外额温计也曾被检测出不合格,被广东省药监局通报。
附:医疗器械飞行检查结果
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/EsP6m4CbooNCsv0qaqPj0Q)



