抢首仿,靠的不是速度!!
8月5日,NMPA发布的通知件中,成都康弘药业的布瑞哌唑口崩片在列。
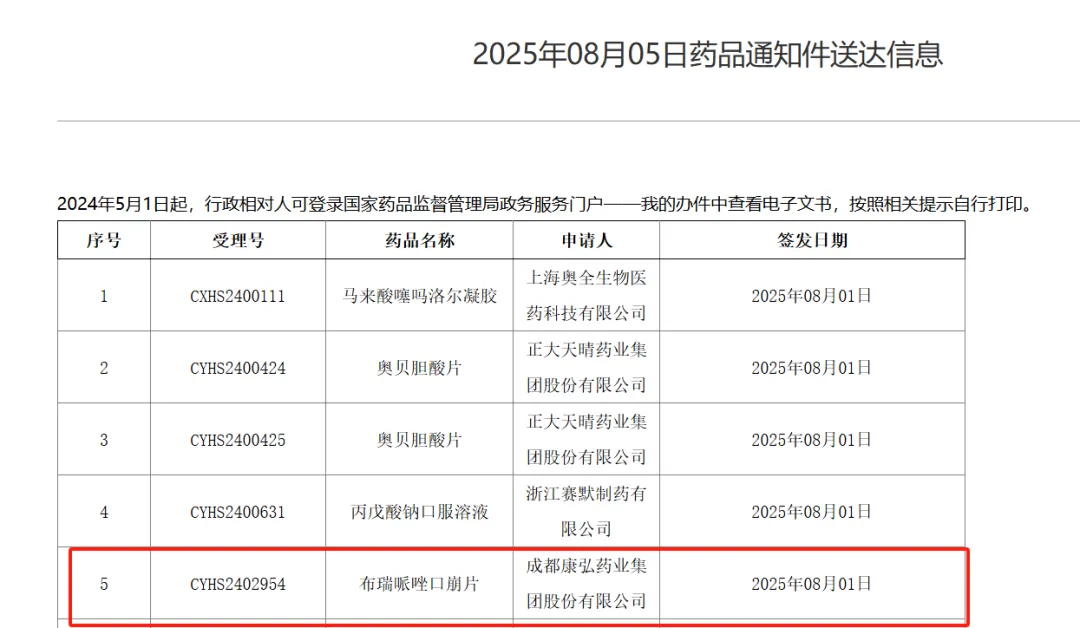
布瑞哌唑,从去年起就备受瞩目。先是片剂短时间内有近六十家布局,后有十几家口崩片口溶膜马不停蹄申请上市。
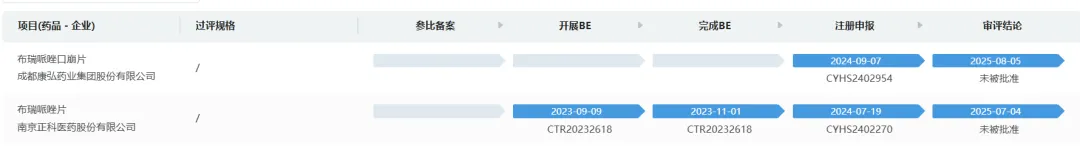
好一番热火朝天的景象,但最近布瑞哌唑片剂和口崩片接连收到通知件,这两家企业都是反应速度快的企业,在历经三百多天评审后,最终却失败了。
01
原研上市不到一月,国内三种剂型就接连申请上市。
布瑞哌唑由大冢制药研发,是第三代抗精神病类药物,优势在于不良反应和停药率更低。
2024年6月25日,大冢制药旗下布瑞哌唑片(商品名:锐思定)在国内获批上市,用于治疗“精神分裂症”。
2024年7月9日,科伦的布瑞哌唑口崩片的上市申请被受理,3类申报;同一日,科伦的布瑞哌唑口溶膜按照2.2类申报上市;7月10日,布瑞哌唑普通片的上市申请被受理,4类申报。
7月18日,齐鲁的布瑞哌唑口崩片和普通片上市申请被受理,7月19日,齐鲁的布瑞哌唑口溶膜同样按照2.2类申报上市。
这两家企业同成分三个剂型报产时间几乎一致,显然资料早就准备好了,科伦先打头阵,齐鲁跟进,赌得就是布瑞哌唑这一成分有效性和安全性已被证实,增加剂型不需要做大临床。
仔细去查一下数据,以锐思定上市时间为节点,国内就有16家企业完成了布瑞哌唑片的BE试验,就等着原研获批上市,到7月底,布瑞哌唑片就新增了6家企业的上市申请。
仿制速度是卷起来了,但首仿成功的消息一直没传来,驳回的记录倒是有了好几条。
成都苑东和重庆药友在2020年原研还没有国内上市时,以3类仿制申请上市,2021年相继收到通知件,2024年7月,两家公司抓紧重新以4类进行了申报,正在审评中。
哈尔滨三联药业在2024年8月23日提交申报,一个月之后就驳回了,推断是撤回了。
南京正科是首家经历了技术评审后被驳回的企业,在第一轮审评完后即被拒批,没给发补的机会,从已有BE登记信息猜测可能是BE方案存在问题。
成都康弘药业集团股份有限公司的布瑞哌唑口崩片在历经三百多天评审之后也被驳回了,同样没给发补机会。
成都康弘药业的口崩片BE试验登记很早,选择的是普通片作为对照药,而齐鲁等公司选择的是日本上市的布瑞哌唑口崩片作为对照药,推测也是BE方案问题。
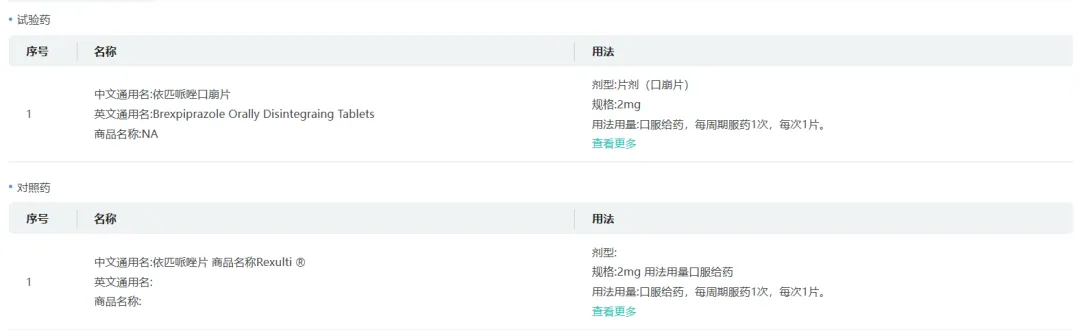
口溶膜倒是暂时没有企业被驳回,科伦和齐鲁都进入了补充资料阶段,齐鲁已经反超科伦,7月1日已提交了补充资料,而科伦尚无发补进度。

类似的报产速度竞赛近些年屡见不鲜,现如今已经卷到了原研上市后7天内CDE就能受理企业仿制上市申请。
虽然业内一直贬低仿制药的技术难度,认为仿制药获批轻而易举,但多家企业的驳回记录告诉我们,上市申请光有速度没有质量,只会得不偿失。
*声明:本文内容转载于网络,版权归原作者所有,转载目的在于传递信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除!
(https://mp.weixin.qq.com/s/zjZE4_Y_iaug00wjpLv18g)



